Durch verschiedenste, immer weiter entwickelte Methoden in der elektrophysiologischen Forschung sind viele neurowissenschaftliche Phänomene gut verstanden. Es gibt unterschiedlichste Messmethoden zur Untersuchung der elektrophysiologischen Eigenschaften von erregbaren Zellen.
In diesem Modul werden intrazelluläre Messungen im Soma von einzelnen Nervenzellen simuliert.
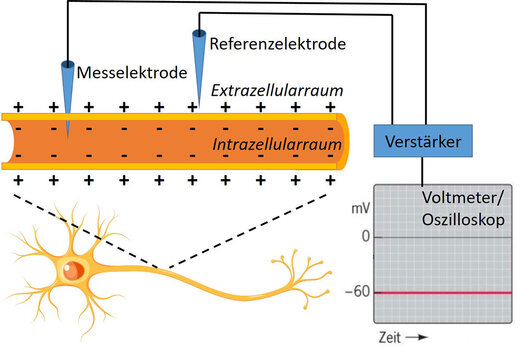
Du kennst diese Messung von der Ableitung des Membranpotenzials von Nervenzellen (Abbildung 5). Dazu benötigt es neben einer Mikroelektrode im Intrazellularraum (Messelektrode) eine zweite Referenzelektrode im Extrazellularraum, um die Ladungsdifferenz bestimmen zu können. Die gemessene Spannung wird von einem Verstärker übertragen und kann auf einem Oszilloskop oder Computer angezeigt werden.
Nach Definition gilt, das Potenzial ist die Ladungsdifferenz vom Innenmilieu im Vergleich zum Außenmilieu. Die Spannungsänderungen werden vom Oszilloskop mit Auslenkungen in senkrechter Richtung angezeigt (Amplitude).
Je nach Gegebenheiten und Untersuchungsbedarf, wird die intrazelluläre Elektrode unterschiedlich in der Zelle platziert. Grundsätzlich können Ableitungen von allen Abschnitten der Zelle von Interesse sein, da sich die Potenzialveränderungen am Soma anders verhalten, als am Axon. Bei vielen Zellen sind die Nervenfasern jedoch so dünn, dass eine Ableitung am Soma zu bevorzugen ist. Viele Untersuchungen am Axon wurden an den Riesenaxonen der Tintenfische durchgeführt, da diese einen Durchmesser von bis zu 1 mm aufweisen.
Um in einem Forschungslabor Messungen von Membranpotenzialen der Zellen des Blutegel-Ganglions durchzuführen, benötigt es einen aufwendigen Versuchsplatz (elektrophysiologisches Setup, Abbildung 6 A). Neben den bereits genannten Komponenten, wird das vorher isolierte Ganglion auf einem speziellen Objektträger befestigt und mit einer physiologischen Salzlösung umspült, welche das Außenmilieu ersetzt (Abbildung 6 B). Der Einstich der Mikroelektrode erfolgt über die manuelle Steuerung eines Mikromanipulators, der die Elektrode in feinen Schritten bewegt. Neben dem Versuchsplatz stehen diverse Messgeräte, z. B. ein Speicheroszilloskop zum Aufzeichnen der Spannungsmessungen. Für die elektrische Abschirmung ist ein Faradaykäfig notwendig, da die Spannungsänderungen sehr klein sind (im Millivolt Bereich). Die Mikroelektroden werden aus Glaskapillaren hergestellt, deren Spitze mit einem sogenannten Elektroden-Ziehgerät ausgezogen wird (Abbildung 6 C). Die Methode ermöglicht, Elektrodenspitzen zu erhalten, deren Durchmesser wenige Nanometer beträgt (1 nm = 10-9 m). Das ist wichtig, damit im Speziellen bei intrazellulären Messungen keine großen Schädigungen in der Zelle durch die mechanische Einwirkung entstehen.

Die physiologische Badlösung, die im Versuchsaufbau das zu untersuchende Gewebe umspült, kann im Experiment verändert werden. Beispielsweise können Neurotransmitter der Badlösung zugesetzt werden (Badapplikation), um zu untersuchen, wie die jeweilige Zelle darauf reagiert (Abbildung 7). Hierbei erfolgt eine langsamere Diffusion in das Segmentalganglion und eine Aktivierung aller Rezeptoren. Durch die Diffusionsprozesse setzt die Reaktion der Zelle (wenn vorhanden) verzögert ein.
Eine andere Möglichkeit ist die Applikation über eine Injektionselektrode, bei der die Substanz in der Elektrode über einen vermittelnden Strompuls herausgedrückt wird (lokale Applikation, Abbildung 8). Der Vorteil dieser Methode liegt darin, dass ein schnellerer Effekt ausgelöst werden kann und die zu untersuchenden Strukturen genauer gewählt werden können (z. B. Rezeptoren in synaptischer Region). Der Nachteil ist, dass es methodisch deutlich anspruchsvoller ist. Beide Methoden ermöglichen eine genauere Untersuchung von Neurotransmitter-Rezeptoren, indem unterschiedliche Agonisten appliziert werden.
Agonisten sind Moleküle, welche durch die spezifische Besetzung eines passenden Rezeptors (Schlüssel-Schloss-Prinzip) die Signaltransduktion in der zugehörigen Zelle aktivieren. Es kann sich sowohl um spezifische körpereigene Liganden (Hormone oder Neurotransmitter), als auch um körperfremde Wirkstoffe (imitieren Botenstoffe in ihrer Wirkung) handeln. Anhand der Intensität der Aktivierung des Rezeptors findet eine Unterteilung in volle Agonisten, partielle Agonisten und Superagonisten statt.